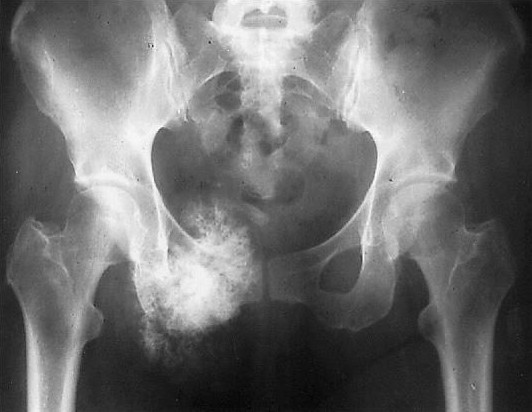
Саркома юинга тазобедренного сустава 4 степени
Саркома Юинга (лат. myeloma endotheliale) — злокачественная опухоль костного скелета. Саркома Юинга, как правило, поражает нижнюю часть длинных трубчатых костей, ребра, таз, лопатку, позвоночник и ключицу.
Была открыта Джеймсом Юингом (1866—1943) в 1921 году. Учёный охарактеризовал её как опухоль, поражающую в основном длинные трубчатые кости.
Саркома Юинга является одной из самых агрессивных злокачественных опухолей [1]. До применения системной терапии почти у 90 % больных развивались метастазы. Наиболее частая локализация метастазов на момент первичной диагностики — лёгкие, кости, костный мозг. 14—50 % пациентов к моменту установления диагноза уже имеют метастазы, выявляемые рутинными методами исследования, и гораздо больше больных имеют микрометастазы. Лимфогенное распространение метастазов встречается редко и всегда связано с плохим прогнозом. Редко также имеет место ретроперитонеальное и медиастинальное распространение метастазов. 2,2 % пациентов имеют метастазы в ЦНС при первичной диагностике, и почти все — при генерализации процесса.
Описание заболевания[править | править код]
Распространение заболевания[править | править код]
Для костных сарком характерен быстрый рост и раннее метастазирование. Саркома Юинга является второй по частоте среди злокачественных опухолей костей у детей — составляет 10-15 %. Эта опухоль редко встречается у детей моложе 5 лет и у взрослых старше 30 лет. Пик заболеваемости приходится на 10 −15 лет.
Заболеваемость саркомой Юинга имеет отчетливые географические и этнические особенности. Значительно чаще опухоли этой группы регистрируются у белых подростков по сравнению с жителями стран Африки и Азии. Различия в заболеваемости саркомой Юинга по
половому признаку появляются после достижения больными возраста 13-14 лет. Мальчики болеют чаще, чем девочки в соотношении приблизительно 1,5:1.
В возрасте до 20 лет саркомой Юинга чаще поражаются длинные (бедренная, мало- и большеберцовые, плечевая) кости, в более старшем возрасте – плоские кости таза и черепа, ребра, лопатки, позвонки.
Не менее 70% всех сарком Юинга локализуются на нижних конечностях и в области тазового пояса. Первичное вовлечение в опухолевый процесс костей верхних конечностей, в первую очередь плечевой кости, составляет от 12 до 16%. Более редкими, не превышающими по частоте 10-13%, локализациями саркомы Юинга являются позвонки, ребра, ключицы, лопатки, кости черепа, мелкие кости кисти и стопы.
Причины возникновения[править | править код]
К настоящему времени не удалось выявить потенциальные причины возникновения саркомы Юинга. Существует ряд научных данных, свидетельствующих о роли наследственного компонента в механизме развития заболевания. В частности, описано одновременное развитие
саркомы у сиблингов, что позволяет судить о значении генетических дефектов. Также доказано, что в 40 % случаях возникновение костной саркомы провоцирует травма.[источник не указан 3163 дня]
Саркома Юинга состоит из мелких круглых клеток со скудной цитоплазмой, круглым ядром, содержащим нежный хроматин и слабо просматривающиеся базофильные нуклеолы. В отличие от остеосаркомы, она не продуцирует остеоид.
Идея эндотелиальной природы опухоли Юинга превалировала до 1980 года. Исследования, проведенные в последние годы, показали нейрогенную природу опухоли Юинга. Чаще саркома Юинга является недифференцированной опухолью костей. В специальной литературе появился термин «семейство опухолей типа саркомы Юинга». К нему относят: собственно саркома Юинга; периферические примитивные нейроэктодермальные опухоли (PNET), в том числе PNET костей, и экстраоссальная саркома Юинга.[2]
Клиническая картина[править | править код]
Общие симптомы[править | править код]
Сложность ранней диагностики объясняется отсутствием онкологической настороженности в отношении лиц молодого возраста, стертой клинической симптоматикой, неправильной интерпретацией жалоб больного (например, объяснением их возникновения спортивной или бытовой травмой и т.п.).
- Боль (от момента появления первых болевых ощущений до установления диагноза проходит от 6 до 12 месяцев)
- Первоначально:
- слабая и умеренной интенсивности
- интермиттирующий характер — может самопроизвольно ослабевать и даже полностью купироваться (т.н. «светлые промежутки»)
- не стихает в покое
- усиление по ночам
- отсутствует облегчение при фиксации конечности.
- По мере роста опухоли боль:
- становится интенсивнее
- ограничивает движения в близлежащем суставе вплоть до контрактуры
- нарушает сон
- нарушает повседневную активность
- Первоначально:
- Быстроувеличивающаяся опухоль нередко с патологическим переломом (поздний признак — 3-4 мес)
- Признаки местного воспаления:
- болезненность при пальпации
- гиперемия кожи
- пастозность (отечность) кожи
- локальное повышение температуры
- расширенные подкожные вены
- Синдром общей опухолевой интоксикации
- повышение температуры тела больного (субфебрильная и фебрильная лихорадка)
- снижение веса и аппетита вплоть до кахексии
- слабость
- анемия
- регионарный лимфаденит
- Метастазы
- в лёгочную ткань (чаще всего)
- в костную ткань
- в костный мозг
- отдаленные метастазы (очень редко): в висцеральных органах, лимфатических узлах средостения и забрюшинного пространства, плевре, центральной нервной системе в виде поражения менингеальных оболочек и вещества головного и спинного мозга.
В зависимости от локализации[править | править код]
- При поражении нижней конечности — хромота
- При поражении позвонков:
- радикулопатия
- компрессионно-ишемическая миелопатия с явлениями параплегии,
- нарушением функции тазовых органов (недержание мочи)
- При поражении костей и мягких тканей грудной стенки (в зарубежной литературе носит название опухоли Аскина):
- плевральный выпот
- дыхательная недостаточность
- кровохарканье
Диагностика[править | править код]
- Рентгенография костей, пораженных опухолью и её метастазами
- Рентгенография и КТ легких
- КТ или МРТ участков скелета, мягких тканей и любых других анатомических областей, пораженных опухолевым процессом. Наиболее точно определяет размеры опухоли, её связь с окружающими тканями, сосудисто-нервным пучком, распространение опухоли по костно-мозговому каналу.
- Позитронно-эмиссионная томография (ПЭТ)
- Остеосцинтиграфия. Позволяет диагностировать отдаленные метастазы
- Ангиография
- УЗИ
- Исследование костного мозга (билатеральная трепано-биопсия костного мозга из крыльев подвздошных костей). Особенностью опухолевого процесса саркомы Юинга является изолированное поражение костного мозга при отсутствии метастазов в костях вне зависимости от первичной локализации или размера опухоли
- Биопсия опухоли. Материал получают из участка кости, граничащего с костномозговым каналом или мягкотканного компонента
- Иммуногистохимическое исследование. Практически 100% клеток саркомы Юинга вырабатывают (экспрессируют) на своих мембранах поверхностный гликопротеин СD99 (р30/32MIC2). Определение его экспрессии является убедительным подтверждением клинико-рентгенологического диагноза саркомы Юинга.[3] Кроме того, для клеток саркомы Юинга характерна экспрессия виментина.
- Молекулярно-генетическое исследование.
- Флуоресцентная гибридизация in situ. Практически 90-95% опухолевых клеток имеют транслокацию между 11-й и 22-й хромосомами (t (11;22) (q24;q12)), приводящую к синтезу патологического белка EWS/FLI1 [4]. Определение данного генетического дефекта является патогномоничным симптомом (характерным только для этого заболевания) саркомы Юинга.
- Полимеразная цепная реакция (RT-PCR). Более чувствительный метод. Используется для определения микрометастазов саркомы Юинга в костном мозге и периферической крови.
Гистологическая картина[править | править код]
Классическая гистологическая картина саркомы Юинга представлена бесструктурными агрегатами мелких опухолевых клеток, разделенных фиброзными прослойками. Клетки имеют правильную форму, содержат округлые или овальные ядра, характеризуются высоким ядерно-цитоплазматическим отношением. Заключенная в клеточных ядрах дисперсия хроматина придает им характерный «зеркальный» вид. Митотическая активность в клетках саркомы Юинга, как правило, низкая. Зачастую при патоморфологическом исследовании определяется выраженный некроз опухолевой ткани, с преимущественной локализацией жизнеспособных клеток вокруг сосудов. Особенности морфологии саркомы Юинга затрудняют проведение дифференциальной диагностики с другими мелкоклеточными злокачественными опухолями у детей (нейробластомой, рабдомиосаркомой, неходжкинской лимфомой, синовиальная саркома, лейомиосаркома и др.). Поэтому проведение биопсии недостаточно для постановки диагноза саркомы Юинга [5]
Рентгенологическая картина[править | править код]
- Сосуществование деструктивного и реактивного (остеосклеротического) процессов костеобразования.
- Распространение опухолевого процесса на кортикальный слой вызывает его разволокнение, расслоение, нечеткость контуров, секвестрацию.
- Вовлечение надкостницы стимулирует периостальное костеобразование пластинчатого или игольчатого типа.
- Практически всегда имеется мягкотканный компонент опухоли, по размерам нередко превосходящий участок первичной костной деструкции.
- Характерна однородная структура мягкотканного опухолевого компонента, без элементов патологического костеобразования, обызвествлений или хрящевых включений
Магнитно-резонансная томография[править | править код]
- метод выбора при стадировании опухоли
- оценка ответа на химио- лучевую терапию
- позволяет оценить поражение мягких тканей
- низкий сигнал на Т1 взвешенных изображениях
- гетерогенное контрастное усиление
- гетерогенно высокий МР сигнал на Т2 взвешенных изображениях
Лечение[править | править код]
- Многокомпонентная химиотерапия (используются препараты — винкристин, адриамицин, ифосфамид, циклофосфан, актиномицин, вепезид в комбинации). В современных программах лечения применяется предоперационная и послеоперационная полихимиотерапия, при этом учитывается также гистологический ответ опухоли на лечение. Хорошим ответом опухоли на химиотерапию считается наличие менее 5 % живых опухолевых клеток[источник не указан 3163 дня].
- Лучевая терапия на очаг в высоких дозах. При развитии метастазов в лёгкие проводится лучевая терапия на лёгкие.
- Если возможно, радикальное удаление опухоли (включая кость и мягкотканный компонент). Радикальная резекция возможна при очаге в малоберцовой кости, костях предплечья, ребрах, ключице, лопатке.
Операция улучшает локальный контроль опухоли. В сочетании с интенсивной химиотерапией и лучевой терапией значительно снижается риск местного рецидива. Уменьшение частоты местного рецидива отмечается даже после нерадикальных операций. Современная хирургическая техника позволяет проводить органосохраняющие операции при поражении бедренной, плечевой костей, а также резекцию костей таза.
Пациентам с плохим прогнозом, в частности с метастазами в кости и костный мозг, имеющим выживаемость менее 10 %, в последнее время назначают более интенсивное лечение — химиотерапия мегадозами препаратов с тотальным облучением тела и трансплантацией аутологичного костного мозга или периферических стволовых клеток. Эта терапия позволяет излечить более 30 % больных с распространенным процессом (при метастазах в кости и костный мозг). У больных с хорошей чувствительностью опухоли удается достичь ещё более высоких результатов лечения (7-летняя выживаемость составляет около 50 %).
Литература[править | править код]
- О саркоме Юинга на medline.ru
- Саркома Юинга (недоступная ссылка) Пер. с англ. Н. Д. Фирсовой (2017)
- Саркома Юинга у детей
См. также[править | править код]
- Карцинома
- USP6
Ссылки[править | править код]
- Сайт Противоракового Общества России
- Radiographia
Примечания[править | править код]
- ↑ Medline.ru — Биомедицинский журнал
- ↑ Архивированная копия (недоступная ссылка). Дата обращения 30 сентября 2012. Архивировано 3 сентября 2013 года.
- ↑ Kovar H., Dworzak M., Strehl S. et al. Overexpression of the pseudoautosomal gene MIC2 in Ewing’s sarcoma and primitive neutoectodermal tumor // Oncogene. – 1990. – Vol.5. – P.1067.
- ↑ de Alva E., Kawai A., Healey J.H. et al. EWS-FLI1 fusion transcript structure is an independent determinant of prognosis in Ewing’s sarcoma // J. Clin. Oncol. – 1998. – Vol.16. – P.1248.
- ↑ Fletcher C.D., Unni K.K., Mertens F. Pathology and genetics of tumors of soft tissue and bone. – Lyon: IARC Press, 2002.
Источник
Рак тазобедренного сустава – это групповое понятие, подразумевающее злокачественные новообразования костной и хрящевой тканей в области сочленения подвздошной и бедренной кости.
Рак этой локализации встречается у 1% из числа больных, имеющих злокачественные опухоли. Он не имеет выраженного преобладания у лиц разного возраста и пола. Отмечена низкая выживаемость, так как в 70% случаев болезнь диагностируют на стадии отдалённых метастазов.
Этиология
Заболевание развивается, когда у одной или нескольких клеток нормальной кости или хряща в процессе деления появляются мутации. Из-за изменения в генах клетки перестают реагировать на химические сигналы организма, быстро и бесконтрольно делятся, разрушая прилежащие ткани.
После попадания атипичных клеток в кровеносные и лимфатические сосуды они переносятся в другие органы и делятся там – появляются метастазы.
Неизвестна конкретная причина, почему изменяется генетический аппарат клетки, но выявлены факторы, повышающие вероятность такой трансформации:
- Плохо залеченные переломы, с образованием крупной костной мозоли или ложного сустава.
- Наличие в семье случаев заболевания.
- Длительное радиационное воздействие низкой интенсивности, в том числе на рабочем месте.
- Лучевая терапия другой злокачественной опухоли.
- Канцерогены, тропные к костной ткани: бериллий и фосфор.
- Остеомиелит, артрит, туберкулёз кости, периостит и другие воспалительные процессы.
Виды злокачественных опухолей
В зависимости от клетки-предшественника в области тазобедренного сустава могут развиваться несколько видов новообразований.
Остеогенная саркома
Происходит из остеоцитов – клеток кости. Её характеризует быстрый злокачественный рост в окружающие ткани и появление отдалённых метастазов в других частях скелета. Чаще диагностируется в периоды от 10 до 17 и 25-30 лет. Среди заболевших преобладают мужчины.
Остеогенная саркома тазобедренного сустава
Она интенсивнее растёт за пределы кости. Разные гистологические варианты отличаются плотностью, цветом. Характерно наличие многочисленных кровоизлияний и некрозов. При разрастании вызывает тупые постоянные боли в области сустава. Позже деформирует его, мешает движениям. Может дать толчок к началу злокачественной трансформации клеток капсулы сустава – синовиальной саркоме.
Хондросаркома
Разрастание атипичной хрящевой ткани. Чаще всего развивается на фоне энхондромы и остеохондромы – доброкачественных новообразований. Существуют центральная, периферическая и юкстакортикальная формы опухоли. Страдают в основном люди пожилого возраста, одинаково мужчины и женщины.
Визуально ткань выглядит как хрящ, но с бугристой поверхностью, желтоватыми вкраплениями и участками некроза. При увеличении она разрушает кость, деформирует сустав, что вызывает боль и нарушения движений в суставах. Есть опасность принять ранние симптомы за артрит и запустить процесс.
Саркома Юинга
Иное название – диффузная эндотелиома кости. Чаще заболевают дети 10-15 лет, мальчики в полтора раза чаще, чем девочки. Частым провоцирующим фактором является перлом. Случаи травмы находят в анамнезе у 40% заболевших. В большинстве случаев опухоль растёт в средней части кости, а в тазобедренном суставе проявляются метастазы. Повреждается костный мозг.
Опухоль серо-белого цвета, мягче и рыхлее, чем кость. В толще встречаются кистовидные полости, очаги некроза и кровоизлияния. Так как узел растёт преимущественно в сторону костномозгового канала, долгое время нет выраженных симптомов, помимо незначительного общего недомогания.
Саркома Юинга тазобедренного сустава
Стадии злокачественного процесса
Первые стадии рака тазобедренного сустава не имеют ярко выраженной клинической симптоматики и диагностируются редко. Для каждого вида рака существует своя градация по стадиям по системе TNM, но по общим признакам выделяют следующие степени процесса:
- 1А – высокодифференцированная опухоль. Клетки похожи по строению на предшественников. Узел ограничен естественным барьером (надкостницей или базальной мембраной), метастазы отсутствуют.
- 1В – высокодифференцированная, прорастает за барьерный слой, но не даёт метастазов.
- 2А – низкодифференцированная опухоль. Клетки бластного типа. Узел ограничен естественным барьером, нет метастазов.
- 2В – низкодифференцированная ткань, прорастающая за барьер, не метастазирующая.
- 3 – регионарные и отдалённые метастазы высоко- или низкодифференцированной опухоли.
Симптомы
Рост новообразования сопровождается появлением общих и местных симптомов. Общие проявления – следствие того, что атипичная ткань воспринимается организмом как чужеродная, и активирует иммунную систему. Также клетки выделяют продукты обмена, вызывая интоксикацию.
Общие симптомы:
- потливость;
- бессонница;
- похудение при неизменном рационе;
- небольшое, но стойкое повышение температуры;
- утомляемость;
- пониженный эмоциональный фон;
- тошнота, потеря аппетита;
- запор;
- увеличение паховых, подколенных лимфоузлов;
- онемение в ногах;
- понижение уровня сывороточного гемоглобина;
- повышение уровня кальция в крови.
Местные симптомы развиваются из-за непосредственного воздействия на окружающие ткани. Они страдают от механического сдавления, от нехватки питательных веществ и выделяемых раковыми клетками токсинов.
Проявления болезни на разных стадиях
Для этой группы патологических процессов выделяют 4 стадии. Стадирование происходит с учётом размеров узла, темпов его роста, инвазии в прилежащие ткани, наличия и локализации метастазов. Для сарком бедренного сустава характерны одинаковые местные симптомы.
- Первая стадия. Определяется, когда есть один локализованный узел размером до 9 см. в наибольшем измерении. Характерен медленный рост, метастазов и отсевов нет. Боль слабая, нелокализованная, ноющая. Иррадиирует ниже по конечности, в ягодицу и крестец на стороне поражения. Не купируется анальгетиками, усиливается при физических нагрузках и в ночное время. Может развиться воспаление бедренного или седалищного нерва.
- Вторая стадия. Размер опухоли превышает 9 см., темпы роста увеличиваются. Метастазы отсутствуют. Боль выражена сильнее, усиливается при движении в суставе, пальпации. отёк сустава и нижней конечности. Видимая деформация сустава. Уменьшение объёма активных движений. Кожные покровы над суставом гиперемированные, пронизаны видимыми венами.
Опухоль тазобедренного сустава
- Третья стадия. Характеризуется регионарным метастазированием в подколенные, паховые лимфоузлы, поверхностные и глубокие, таз. Возможно контактное метастазирование в суставную сумку, отсевы в бедренную кость с образованием дочерних узлов. Боль оценивается человеком как мучительная. Провоцирует хромоту, снижение активности. Видимая деформация сустава, артрит. При пункции в суставной жидкости обнаруживается кровь. Из-за метастазов в полости таза нарушается стул, мочеиспускание. Могут развиваться запоры или недержание мочи и кала. У мужчин характерный симптом– эректильная дисфункция. Патологические переломы бедра. Кость, замещенная опухолевой тканью, может сломаться под весом тела.
- Четвёртая стадия. Ставится при наличии отдалённых метастазов – опухолевого роста в других органах. Чаще всего саркома метастазирует в лёгкие, печень, другую кость. Боли достигают предела переносимости. В ряде случаев не купируются наркотическими анальгетиками. Кашель – проявление метастазов в лёгких. Также сохраняются симптомы предыдущих трёх стадий.
Диагностика
На первых этапах диагностики требуется дифференцировать саркому от воспаления сустава, последствий травмы или проявлений радикулита. Это важно, чтобы определить болезнь на начальной стадии. При наличии метастазов смертность от рака тазобедренного сустава составляет 80%.
Виды обследований:
- Сбор жалоб и анамнеза. Врач узнаёт возраст пациента, случаи травм нижней конечности. Интересуется, была ли патология у членов семьи. Уточняется характер болей, сколько человек может пройти, не захромав. Должны учитываться и признаки общего недомогания: утомляемость, похудение, хронически повышенная температура – все эти признаки могут указывать на злокачественный процесс.
- Осмотр и пальпация. Обращается внимание на изменение формы сустава, болезненность. Можно определить уплотнения по ходу суставной капсулы, неровности на бедренной кости. Исследуются лимфоузлы: их размеры, консистенция, подвижность и болезненность.
- Рентгенография. Ткань саркомы менее плотная, чем у окружающей кости, поэтому на снимке видны тёмные, нечётко очерченные участки. При хондросаркоме в толще узла могут определяться плотные отложения кальция. Часто узел имеет ячеистую структуру из-за сохранившихся в опухоли перегородок. Надкостница над поражённым участком утолщенная, плотная, слоистая. При прорастании опухоли сквозь кость наблюдается симптом «козырька» – костная ткань образует почти горизонтальный вырост над узлом саркомы. Необходимо выполнить рентген всего скелета и прицельно – грудной клетки, для обнаружения метастазов. В лёгких они будут определяться как очаговые резкие уплотнения. Рентген не даёт возможности с точностью оценить размер опухоли, поэтому необходимы более информативные методы.
- УЗИ. Позволяет оценить состояние полости сустава, поверхность хрящей.
- Компьютерная и магнитно-резонансная томография. Методы определяют изменения плотностей тканей, обладают малым шагом и позволяют оценить размеры новообразования с точностью до миллиметра.
- Остеосцинтиграфия. Введение в кровь растворов радионуклидов – изотопов кальция, которые накапливаются в здоровой кости либо опухоли. После этого исследуют интенсивность излучения элементов. Таким образом, можно оценить, насколько активен метаболизм опухоли, и уточнить тип клеток. Это исследование хорошо выявляет метастазы и отсевы опухоли.
- Ангиография. В кровь вводится рентгеноконтрастное вещество и смотрят, как оно распределяется по сосудам. Выясняется, как кровоснабжается опухоль, где пролегают крупные сосуды, которые могут создать осложнения при операции.
- Гистологическое и цитологическое исследование. Берутся образцы тканей. Только после этого может быть окончательно верифицирован диагноз и установлен вид рака. При низкодифференцированных вариантах необходимо применение дополнительных окрасок и генотипирование.
Лечение
Лечение подбирается врачом-онкологом в зависимости от вида, стадии, наличия региональных или отдалённых метастазов. Большую роль играют общее состояние здоровья и возраст пациента. У людей пожилого возраста или при наличии тяжёлых сопутствующих патологий рак 3-4 стадии признаётся инкурабельным, то есть не подлежащим радикальному лечению.
В таком случае больному назначается паллиативное лечение, направленное на продление и улучшение качества жизни. Паллиативное и радикальное лечение включают следующие методы.
Химиотерапия
Введение препаратов, сдерживающих деление и вызывающих гибель опухолевых клеток.
Виды химиотерапии:
- Предоперационная – способствует уменьшению размеров узла и метастазов, предотвращает дальнейшие отсевы. За счёт этого уменьшается объём будущей операции.
- Послеоперационная – в процессе удаления узла всегда присутствует опасность оставления отдельных опухолевых клеток или занесение их на здоровые ткани, и рак будет прогрессировать. Чтобы снизить риски, химиотерапию не прекращают после вмешательства.
- Профилактическая – для предотвращения отдалённых рецидивов.
- Лечебная – часть паллиативного лечения. Сдерживает рост злокачественных клеток.
Препараты: Ифосфамид, Вепезид, Доксорубицин, Цисплатин. Применяют инъекционные и таблетированные формы.
Химиотерапия проводится циклами по 7-10 месяцев, поскольку нацелена на бесконечно делящиеся клетки.
Лекарства для терапии рака предназначены для уничтожения клеток, поэтому могут поражать здоровые клетки. Эффект усугубляется токсинами, которые выделяют гибнущие раковые клетки. Возникают побочные проявления:
- Тошнота и рвота.
- Облысение.
- Гемолитическая анемия.
Хирургическое лечение
Основной метод лечения сарком тазобедренного сустава. Объём резекции зависит от стадии процесса. Во время операции новообразование удаляется в пределах здоровых тканей. Удаляется суставная сумка, часть бедренной кости и ткани вертлужной впадины подвздошной кости. Одновременно иссекаются все регионарные лимфоузлы. При наличии отдалённых метастазов подход зависит от того, какой орган поражён. После завершения лечения устанавливается искусственный сустав.
В запущенных случаях заболевания проводится ампутация нижней конечности. Также на 3-4 стадии заболевания показана трансплантация костного мозга.
Лучевая терапия
Клетки саркомы тазобедренного сустава малочувствительны к облучению, поэтому оно показано при опухолях на 1-2 стадии либо как элемент паллиативного лечения. После курса лечения человек состоит на диспансерном учёте у онколога 5 лет. В течение этого периода осмотры проводятся 3-6 раз в год.
Прогноз выживаемости
Продолжительность жизни после операции зависит от вида и стадии рака. При остеосаркоме и хондросаркоме 1-2 стадии пятилетняя выживаемость составляет 70%. При саркоме Юинга 3-4 стадии прогноз неблагоприятный: выживаемость падает до 10%.
Профилактика рака
Так как этиология раковых заболеваний не выяснена, нет 100% действенных способов профилактики. Выполнение рекомендаций ВОЗ поможет снизить вероятность развития опухоли или повысит шансы выздороветь.
- Сбалансированное питание и контроль массы тела.
- Отказ от вредных привычек.
- Лечение травм сустава и бедренных костей.
- Удаление доброкачественных опухолей кости.
- Уменьшение контакта с источниками радиации.
- Избегание канцерогенов.
И главное – своевременное обращение к врачу при возникновении настораживающих симптомов: боли в ноге на фоне общей слабости и ухудшения самочувствия.
Выберите город, желаемую дату, нажмите кнопку «найти» и запишитесь на приём без очереди:
Источник
