Накопление рфп в локтевых суставах
Вопрос №1. Что такое исследование «всего тела»?
Исследование «всего тела» заключается в сканировании пациента от уха до верхней трети бедра. Т.е. в область исследования будут включены голова (частично, от козелка уха, без захвата головного мозга), шея, органы грудной полости, брюшной полости, малого таза и костная система (без верхних и нижних конечностей).
Сканирование нижних конечностей проводится за дополнительную плату.
Вопрос №2. Что такое радиофармпрепарат?
Радиофармпрепарат (РФП) – это соединение, состоящее из специального вещества и радионуклида (изотопа, радионуклидной метки). Специальное вещество отвечает за то, в каком органе накопится РФП, а радионуклидная метка позволяет врачу-диагносту увидеть это накопление на изображении.
В настоящее время для производства РФП используется очень широкий спектр как специальных веществ, так и радионуклидных меток. Во всем мире самым часто используемым у онкологических больных соединением специального вещества и радионуклидной метки является 18F-фтордезоксиглюкоза (18F-ФДГ). В данном соединении 18F выполняет функцию радионуклидной метки, ФДГ – специального вещества.
Вопрос №3. Что такое физиологическое накопление РФП?
Физиологическое накопление (гиперфиксация) РФП – это повышенное накопление РФП, определяющееся в различных органах и системах в норме.
Физиологическое накопление наблюдается при исследованиях со всеми РФП: 18F-ФДГ, 11С-холином, 11С-метионином, 68Ga-ПСМА и т.д. В зависимости от типа РФП меняется лишь местоположение физиологической гиперфиксации. Например, при ПЭТ и ПЭТ/КТ с самой часто используемой 18F-ФДГ физиологическое накопление РФП определяется в коре головного мозга, ротоглотке, носоглотке, мышцах гортаноглотки, миокарде левого желудочка, чашечно-лоханочных системах почек, фрагментарно по ходу петель толстой кишки, мочевом пузыре.
Вопрос №4. Что такое патологическое накопление РФП?
Патологическое накопление РФП – это повышенное накопление РФП в органах и тканях, регистрирующееся при заболеваниях, чаще всего в злокачественных опухолях.
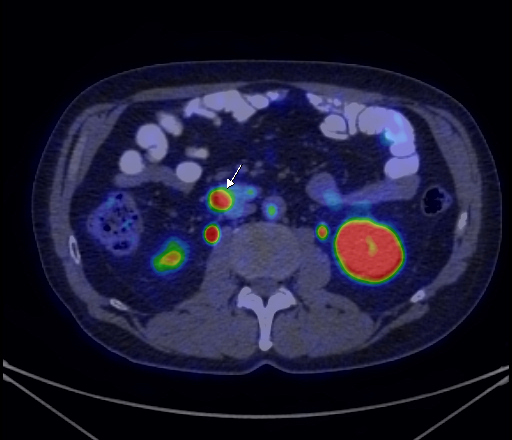 |
| Данные ПЭТ/КТ с 68Ga-DOTA-TATE у пациента с нейроэндокринной опухолью тощей кишки. В проекции злокачественной опухоли, расположенной в тощей кишке, определяется очаг патологической гиперфиксации РФП. |
Вопрос №5. Что такое метаболически активное и метаболически неактивное образование?
Метаболически неактивное образование – это образование, которое не накопило РФП. Чаще всего отсутствие повышенного накопления РФП в опухоли свидетельствует о ее доброкачественной природе.
 |
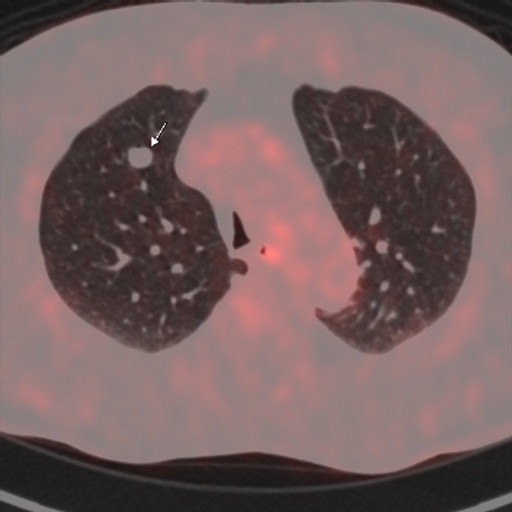
| Данные ПЭТ/КТ с 18F-ФДГ у пациента с метаболически неактивным образованием правого легкого (доброкачественная опухоль — гамартома). |
Метаболически активное образование – это образование, в котором накопился РФП в повышенном количестве. Повышенное накопление РФП в опухоли чаще всего свидетельствует о ее злокачественном характере.
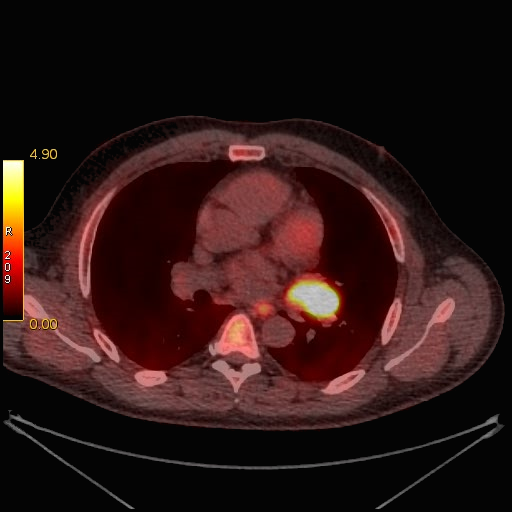 |
| Данные ПЭТ/КТ с 11С-метионином у больного с метаболически активным образованием корня левого легкого (типичный карциноид). |
Вопрос №6. Что такое SUV?
SUV (Standardized Uptake Value, стандартизированный уровень захвата) – это величина, отражающая интенсивность накопления РФП в зоне интереса, например, в опухоли.
Показатель SUV рассчитывается программным комплексом автоматически и измеряется в различных единицах. В нашем Центре, как и в большинстве отечественных и зарубежных медицинских учреждений, где проводится позитронная эмиссионная томография, в качестве единиц измерения показателя SUV принято использовать г/мл (g/ml).
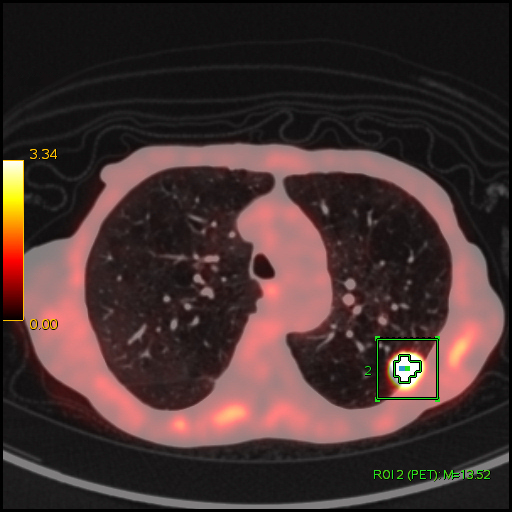 |
| Данные ПЭТ/КТ с 18F-ФДГ. Оконтуривание метаболически активной злокачественной опухоли левого легкого для измерения показателя SUV. В данном случае величина SUV в опухоли определяется на уровне 13,52 g/ml. |
Вопрос №7. Для чего используется величина SUV?
Величина SUV в основном используется для оценки ответа злокачественной опухоли на проведенное лечение. Важно подчеркнуть, что в ряде клинических ситуаций показатель SUV в опухоли является единственным критерием, позволяющим оперативно получить информацию о чувствительности образования к только что начатой терапии.
Если опухоль чувствительна к лечению, то уровень SUV в ней при повторном ПЭТ-исследовании будет снижаться, если нечувствительна или малочувствительна (резистентна, устойчива) – значение SUV останется без изменений или увеличится. Следует помнить, что своевременная диагностика устойчивости опухоли к лечению позволит скорректировать план лечения, а в некоторых случаях и радикально его изменить.
Как уже было сказано выше, для оценки эффективности терапии врач-радиолог оценивает динамику показателя SUV до и после лечения.
Существует четыре варианта метаболического ответа опухоли на проведенное лечение:
- Частичный метаболический ответ – устанавливается при уменьшении значения SUV в опухоли на 25% и более;
- Полный метаболический ответ – заключается в отсутствии повышенного накопления РФП в опухоли;
- Метаболическое прогрессирование – устанавливается при увеличении SUV на 25% и более и/или при появлении новых очагов патологической гиперфиксации РФП;
- Метаболическая стабилизация – регистрируется при отсутствии достоверных (менее 25%) изменений показателя SUV в опухоли.
Результаты ПЭТ с 18F-ФДГ у пациента с диффузной В-клеточной крупноклеточной лимфомой до лечения (а), после 2 курса ПХТ (б) и через 13 месяцев после окончания терапии (в).
а – до лечения в средостении визуализируется массивное метаболически активное образование с уровнем SUV=12,6;
б – после 4 курса ПХТ отмечается значительное уменьшение метаболического объема опухоли и снижение показателя SUV до 3,4 (достигнут частичный метаболический ответ, т.е. опухоль чувствительна к выбранной ПХТ);
в – через 13 месяцев после окончания ПХТ очагов патологической гиперфиксации РФП в проекции органов средостения не обнаружено (достигнут полный метаболический ответ).
Источник
 25.12.2017
25.12.2017
Остеосцинтиграфия в ревматологии: новые подходы к дифференциальной диагностике ревматоидного артрита
Среди обширной группы ревматических заболеваний центральное место занимают ревматоидный артрит (РА) и диффузные болезни соединительной ткани (ДБСТ), названные Е.М. Тареевым “большими коллагенозами” в силу системности поражения и неблагоприятного прогноза.
Среди обширной группы ревматических заболеваний центральное место занимают ревматоидный артрит (РА) и диффузные болезни соединительной ткани (ДБСТ), названные Е.М. Тареевым “большими коллагенозами” в силу системности поражения и неблагоприятного прогноза. В клинической и патоморфологической картине указанных заболеваний преобладают прогрессирующие изменения опорнодвигательного аппарата, которые являются одной из причин потери трудоспособности и ранней инвалидности [3, 7]. Процент диагностических ошибок у больных ревматоидным артритом и диффузными болезнями соединительной ткани достаточно высок, нередко окончательный диагноз ставится спустя несколько лет с момента первого обращения.
Сложность проблемы усугубляется полиморфизмом суставных проявлений, многообразием вариантов течения указанных заболеваний, наличием между ними перекрестных форм и пограничных синдромов [1, 5, 6]. На ранних этапах суставные проявления болезни имеют клинически сходных черт больше, чем различий [2, 4, 8, 11]. Основным методом, позволяющим судить о присутствии и локализации ревматического процесса, его протяженности инозологической принадлежности, по праву считается рентгенологический. Между тем,рентгенологическая картина не всегда в состоянии отобразить начальные изменения в скелете, а из-за больших лучевых нагрузок метод не позволяет одномоментно исследовать все суставы, быстро оценить динамику заболевания в процессе лечения. Поэтому понятен интерес к использованию в ревматологической практике остеосцинтиграфии.
Нами исследовалась чувствительность радионуклидной остеосцинтиграфии с фосфатными комплексами в оценке скелетного метаболизма, обнаружении как первичных поражений суставов, так и субклинического течения артрита у больных РА и ДБСТ, а также в выявлении характерных особенностей накопления и распределения РФП в суставах и костях осевого и периферического скелета, мягких тканях скелета, паренхиматозных органах,что могло бы быть полезным в раннем распознавании и дифференциальной диагностике этих заболеваний.
Исследование и оценка полученных данных проводились по методике, описанной в статье Ю.Н. Касаткина с соавт. (Радиология –практика. 2003. No 3. С. 31–37). Обследовано 427 человек в возрасте от 18 до 64 лет (РА –196, ДБСТ – 231) и 87 больных с неустановленным точным диагнозом изза схожести клинических проявлений. 114 больных ДБСТ страдали системной красной волчанкой (СКВ), системная склеродермия (ССД) диагностирована у 95 человек, дерматомиозит (ДМ) – у 22 больных. У 134 больных (69,4%) РА выявлена типичная форма заболевания, 62 (30,6%) имели системные проявления.
Анализ результатов показал, что общими радионуклидными признаками поражения суставов для обоих заболеваний являются:
1) симметричность процесса с преимущественным поражением периферических суставов по сравнению с суставами осевого скелта;
2) вовлечение в патологический процесс мелких суставов кистей и стоп.
Однако, несмотря на схожесть сцинтиграфических проявлений, у каждого из них имелись особенности, обусловленные различиями патоморфологических процессов, наблюдаемых в костях,суставах, мягких тканях скелета в зависимости от нозологической формы заболевания.
Ревматоидный артрит.
Поражение суставов –главное клиническое проявление ревматоидного полиартрита. Первоначальным и основным клиникоанатомическим проявлением,определяющим дальнейшее течение и прогрессирование заболевания, является воспа лительное поражение синовиальных оболочек сустава с последующей деформацией. Основной иммунный конфликт при РА происходит в синовиальной оболочке сустава. Наряду с ограниченными суставными формами РА (типичный РА), выделен РА с системными или с внесуставными проявлениями, когда ревматоидные полилимфаденопатии, васкулиты и висцериты выступают на первый план уже на ранних этапах болезни. В этих случаях заболевание носит черты одной из форм ДБСТ, и диагностика его чрезвычайно затруднена.
При радионуклидном исследовании скелета в сканографической картине этой группы пациентов основным являлось преобладание воспалительного типа поражения суставов(табл. 1), когда гиперфиксация РФП в области пораженных суставов регистрировалась как в фазе “кровяного пула”, так и на отсроченных (через 3–5 ч) сканограммах с достаточно высоким уровнем активности. Резко положительная степень накопления РФП в пораженных суставах выявлена у 74 пациентов из 196 обследованных больных, умеренно положительная – у 105 больных, слабо положительная – лишь у 17 больных. Очаг воспаления обычно достаточно хорошо контрастируется, внутрисуставные щели деформированы либо совсем не прослеживаются.
Отмечается прямая зависимость сцинтиграфических находок от стадии процесса.
При значительном выпоте в полость сустава с растяжением суставной капсулы контуры его могут быть изменены, эпифизы костей не дифференцируются – сустав определяется в виде пятна, контрастность которого зависит от активности патологического процесса и выраженности его экссудативного компонента.
Места скопления экссудата (полость сустава,суставные сумки) еще более отчетливо выявляются на эмиссионных компьютерных томограммах (рис. 1). Отмеченные изменения, как правило, симметричны, регистрируются в основном в области дистальных отделов конечностей (кистях, стопах) и коленных суставах.
При вовлечении в патологический процесс кистей наиболее ранним сцинтиграфическим признаком является достаточно интенсивное накопление РФП в области запястий и луче запястных суставов. При этом практически постоянно отчетливо визуализируются яркие очаги гиперфиксации РФП в II, III пястнофаланговых, II–IV проксимальных межфаланговых суставах, реже – в пястнозапястных. Дистальные межфаланговые и первый пястнофаланговый суставы вовлекаются в процесс значительно реже и на более поздних стадиях.
В стопах чаще отмечается сочетанное повышение накопления РФП в мелких суставах предплюсны, проекции шопарова и первого плюснефалангового суставов. Наблюдаемое увеличение активности в периферических суставах регистрируется на фоне слабого контрастирования диафизов смежных трубчатых костей. Что касается метаболической активностикостной ткани осевого скелета (свода черепа,таза, позвонков), а также уровней фиксации РФП в мягких тканях скелета и почках, то в преобладающем большинстве случаев они не отличались от нормы (см. табл. 1). Не отмечено также статистически значимого отличия от нормы соотношения интенсивности накопления (ИН) почки с ИН в позвоночном столбе.
По мере развития процесса при обеих формах течения РА почти у всех пациентов, за небольшим исключением, в процесс вовлекались межзапястные, пястнофаланговые, проксимальные межфаланговые, предплюсневые и плюснефаланговые суставы (табл. 2).
На фоне поражения мелких суставов кистей и стоп практически у всех обследуемых больных РА было обнаружено вовлечение в процесс крупных суставов. Факт их поражения на субклиническом уровне в начальных стадиях заболевания устанавливался лишь с помощью меченых остеотропных препаратов. Из крупных суставов наиболее часто поражались лучезапястные, коленные, голеностопные.
В области нижних конечностей чаще обнаруживается сочетанное вовлечение в процесс коленных, голеностопных, мелких суставов предплюсны и плюснефаланговых суставов; в верхних – межзапястных, пястнофаланговых, проксимальных межфаланговых и лучезапястных суставов.
В более поздние сроки возможно повышение активности в дистальных межфаланговых,плечевых, локтевых суставах и других сочленениях осевого скелета. Изменения в суставах позвоночного столба и тазобедренных суставах фиксируются в III–IV стадии заболевания.
В стадии пролиферативнодегенеративных изменений распределение РФП в пораженном суставе может быть в виде отдельных узлов различных размеров, достаточно отчетливо контурируемых, однако накопление в них РФП менее интенсивное, нежели при остром артрите.
В стадии склероза фиксация РФП в очаге поражения уменьшается, однако в связи с тем,что в течении заболевания нет строгой последовательности клиникоанатомических стадий, в пораженных суставах наблюдаются морфологические, а следовательно, и сцинтиграфические изменения, характерные для всех трех стадий.
Сцинтиграфическая картина коленных суставов на разных фазах воспалительного процесса представлена на рис. 2.
В диагностическом плане наиболее значимым было преимущество сцинтиграфии в выявлении субклинических очагов воспаления у больных, в дебюте заболевания которых наблюдался моноартрит либо олигоартрит. Выявление у них дополнительных очагов поражения с типичной для РА локализацией (рис. 3) вкомплексе с результатами клинического обследования, с одной стороны, позволяет врачу правильно поставить диагноз задолго до проявления типичных признаков заболевания, с другой –своевременное предотвращение структурных повреждений, выявленных методом сцинтиграфии на ранних стадиях заболевания, способствует сохранению функциональной активности пациентов в долговременной перспективе. Полученные результаты полностью согласуются с данными литературы о том, что “субклинически” текущий иммунопатологический процесс развивается задолго до появления клинически очевидных признаков артрита, а по данным биопсии синовиальной оболочки сустава признаки хронического синовита выявляются в самом начале болезни даже в клинически непораженных суставах [1, 2, 4].
Диффузные болезни соединительной ткани(ДБСТ).
В соответствии с Международной классификацией болезней, в эту группу включены системная красная волчанка (СКВ), системная склеродермия (ССД), дерматомиозит(ДМ). Важным клиникоморфологическим проявлением заболевания является поражение микроциркуляции, повышение сосудистой тканевой проницаемости, развитие васкулитов.
Суставный синдром у больных ДБСТ протекает на фоне выраженных нервнотрофических расстройств костносуставной системы и периартикулярных тканей (мышц, сухожилий), что в конечном счете обусловливает развитие остеопороза, артропатии, деформации и др.
В сцинтиграфической картине больных ДБСТ по сравнению с РА преобладает дистрофический тип поражения суставов без повышения активности в области пораженных суставов на фазе кровяного пула (см. табл. 1, рис. 4).
Воспалительный тип поражения суставов регистрируется лишь у 20,3% обследуемых, в основном в мелких суставах кистей, реже стоп. В отличие от РА при ДБСТ отмечается более частое вовлечение в процесс суставов осевого скелета – дистальных межфаланговых, подвздошнокрестцовых, тазобедренных, позвоночного столба. Изменения в других суставах, в том числе голеностопных и коленных наблюдаются столь же часто, как и при РА (см. табл. 2).
Сцинтиграфическая картина вовлеченных в процесс мелких суставов кистей и стоп на отсроченных сканах по сравнению с РА более однотипна и проявляется близким по интенсивности накоплением РФП в пястно и плюснефаланговых суставах в сочетании с умеренным увеличением активности в области запястий и предплюсны. При поражении крупных суставов очаги гиперфиксации РФП не имеют четких границ, слабо контурируются. Интенсивность накопления индикатора в очаге максимального накопления индикатора при этом, как правило, слабо или умеренно положительная и в среднем не превышает 9,5%. Резко положительная степень накопления РФП для данной группы обследуемых не характерна. Суставные щели, за редким исключением, не деформированы и достаточно различимы на фоне эпифизов костей, составляющих сустав. Что касается метаболической активности костной ткани осевого скелета, а также внекостной фиксации РФП в почках и мягких тканях скелета, то у 80–85% обследуемых больных ДБСТ она повышена по сравнению с нормой (см. табл. 2).
Своеобразие сканографической картины осевого скелета больных ДБСТ проявляется в превышении нормального уровня фиксации РФП в плоских костях черепа, таза, почках, пяточных костях стоп (шпоры, энтезопатии), выраженной негомогенностью распределения РФП в области позвоночного столба, на фоне которой дифференцировать структурные элементы отдельных позвонков, преимущественно грудного отдела, невозможно (рис. 5, 6).
Указанные изменения области позвоночного столба у значительной части обследуемых обнаруживаются у молодых больных в возрасте до 25 лет, что не позволяет говорить о банальном сочетании воспалительного и инволютивно дистрофического поражения позвоночника и суставов. Поэтому обнаружение этих изменений у молодых лиц с подозрением на ДБСТ может расцениваться как значительный момент для подтверждения диагноза. Естественно, что с возрастом дифференциально-диагностическое значение этого синдрома утрачивается.
Особенности изученной и систематизированной нами радионуклидной семиотики поражения опорнодвигательного аппарата при РА и ДБСТ были использованы в качестве дифференциальнодиагностических тестов в комплексе с общеклиническими у 87 больных, у которых точная дифференциальная диагностика с использованием общепринятых и дополнительных методов исследования при поступлении больных в клинику была невозможной из-за схожести клинических проявлений. Ре
зультаты в этой группе: число истинноположительных значений – 62%, истинноотрицательных – 18,6%, точность диагностики – 80,4%.
Таким образом, радионуклидное исследование опорнодвигательного аппарата в комплексе с общеклиническими и рентгенологи
ческими данными позволяет выработать дополнительные объективные критерии для диагностики и дифференцирования различных поражений скелета при клинически сходных вариантах их течения и снизить число ошибочных заключений.
Список литературы
1.Беневоленская Л.И.Избранные лекции по клинической ревматологии // Учебное пособие для слушателей институтов и факультетов последипломного образования. М., 2001. 106 с.
2.Насонова Е.Л.Почему необходима ранняя диагностика ревматоидного артрита? // Рус. мед. журн. 2002.Т. 10. No 22. С. 1009–1012.
3. Фоломеева О.М., Лоборева Л.С., Ушакова М.А. и др.Инвалидность, обусловленная ревматическими заболеваниями, среди жителей Российской Федерации // Научнопрактическая ревматология. 2001.No 1. С. 15–21.
4.Dellbare F., Meri K. Критерии для диагностики системных воспалительных ревматических заболеваний // Тер. архив. 1990. No 8. С. 71–81.
5. Emery P., Breedveld F.C., Dougads M. et al. Early refferedrecommendation for newly diagnosed rheumatoid arthritis: evidence based development of a clinical guide //Ann. Rheuv. Dis. 2002. V. 61. P. 290–297.
6.Homme M.H.Collagen disease. Its diagnosis, pathogenesis and treatments // Jap. Medicine. 1981. V. 20. No 3.P. 232–238.
7.Scott D.L. The diagnosis and prognosis of early artritis:rational for new prognostic criteria // Artritis Rheum.2002. V. 46. P. 286–290
Теги: остеосцинтиграфия
234567
Начало активности (дата): 25.12.2017 19:00:00
234567
Кем создан (ID): 989
234567
Ключевые слова:
ревматология, артрит, кости, скелет, ткани, сцинтиграфия
12354567899
Источник
